Microbiome cutané et intestinal : rôle, dysbiose et maladies de peau
Le corps humain abrite 30 000 milliards de bactéries, soit autant que de cellules humaines. Ces micro-organismes ne sont pas des envahisseurs : ils constituent une partie intégrante de notre biologie, formant des écosystèmes indispensables à notre santé — notamment à celle de notre peau.
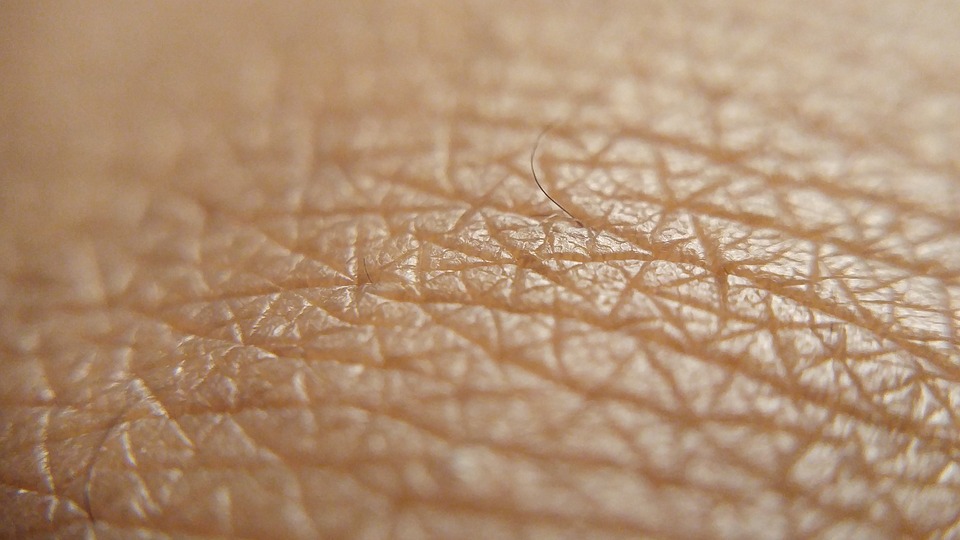
Le microbiome cutané (ou microbiote de la peau) est l’ensemble des micro-organismes vivant à la surface et dans les couches superficielles de la peau : bactéries, virus, champignons, acariens et archées.
Le microbiome intestinal, anciennement appelé flore intestinale, est considéré comme un organe à part entière, pesant près de 2 kilogrammes, et influence profondément la santé cutanée à distance via l’axe intestin-peau.
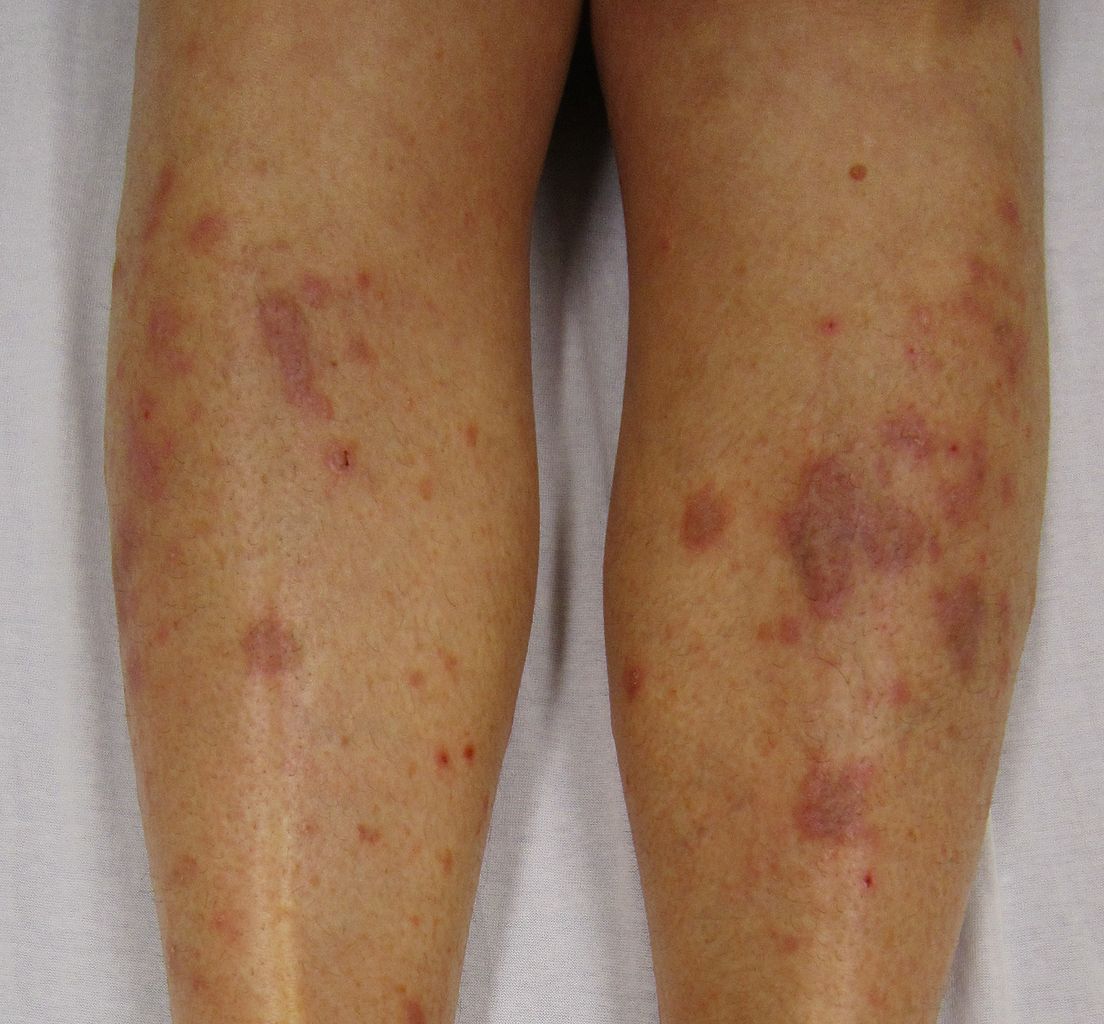
Comprendre ces deux écosystèmes et leurs interactions est devenu fondamental en dermatologie moderne : dysbiose cutanée et intestinale sont impliquées dans l’acné, la dermatite atopique, le psoriasis et la rosacée.
Besoin de l’avis d’un spécialiste ? Délais de rendez-vous trop longs ? Vous pouvez effectuer une téléconsultation avec le dermatologue.
Le microbiome cutané : composition et organisation

La peau d’un adulte s’étend sur environ 2 m² pour un poids de 3 à 5 kg. Sa surface est colonisée par des milliards de micro-organismes dont la composition varie selon les zones anatomiques, le pH local, la densité en glandes sébacées et sudorales, et le niveau d’humidité.
Composition du microbiome cutané :
– Bactéries (espèces dominantes),
– virus : jusqu’à 1 million de particules virales par cm²,
– champignons (Malassezia spp. principalement),
– acariens (Demodex folliculorum dans les follicules pileux),
– archées (micro-organismes ancestraux).
Répartition bactérienne par phyla :
– 50 % Actinobacteria : corynébactéries, Cutibacterium acnes,
– 25 % Firmicutes : staphylocoques, streptocoques,
– 25 % Proteobacteria et Bacteroidetes : entérobactéries, Pseudomonas, Roseomonas, bacilles anaérobies.
Un microbiome unique comme une empreinte digitale :
Chaque individu possède un microbiome cutané qui lui est propre, constituant une véritable signature personnelle, influencée par la génétique, l’alimentation, le mode de vie, l’environnement et l’état de santé.
Les trois grandes zones géographiques cutanées
La composition du microbiome varie selon les caractéristiques physico-chimiques de chaque zone :
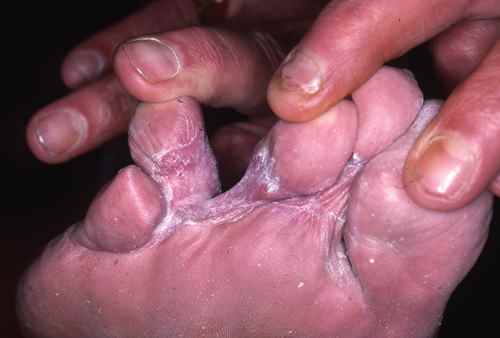
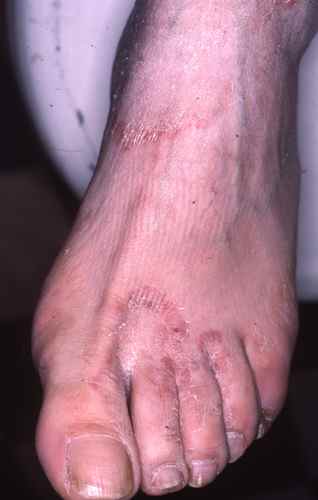
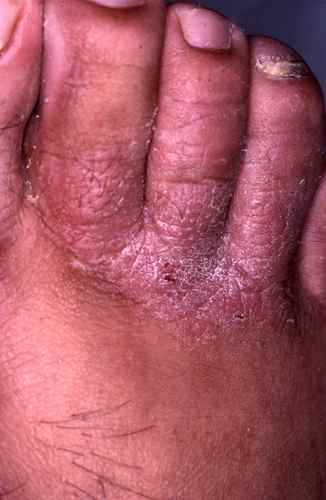
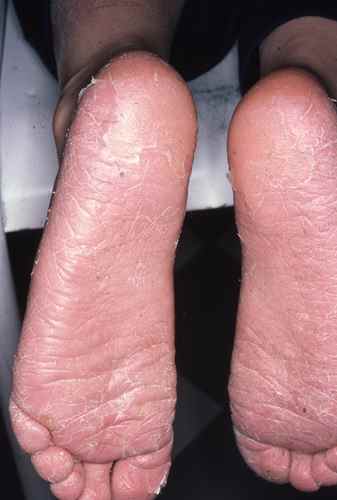
Zones humides (aisselles, aines, espaces interdigitaux) :
Riches en glandes sudorales, pH plus élevé, favorables aux Staphylococcus et Corynebacterium. Ces zones constituent de véritables gîtes microbiens.
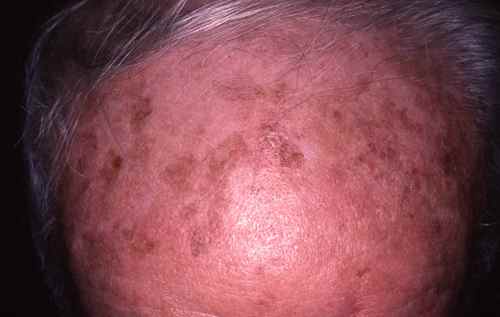
Zones séborrhéiques (visage, cuir chevelu, haut du dos) :
Riches en glandes sébacées, pH acide, dominées par Cutibacterium acnes (anciennement Propionibacterium acnes) qui métabolise les triglycérides du sébum.
Zones sèches (mains, avant-bras, fesses) :
Pauvres en nutriments microbiens, dominées par les Proteobacteria et une diversité bactérienne plus faible.
Les deux types de microbiomes cutanés
Microbiome résident :
Stable, adapté aux conditions cutanées, composé de staphylocoques à coagulase négative (S. epidermidis), corynébactéries, microcoques, Cutibacterium acnes. Il joue un rôle protecteur actif.
Microbiome transitoire :
D’origine digestive ou par contact environnemental, non adapté aux conditions cutanées, éliminé par les défenses naturelles de la peau. En cas de fragilisation de la barrière cutanée (eczéma, plaie), il peut coloniser durablement et provoquer des infections.
Maturation du microbiome cutané de la naissance à l’âge adulte
Le microbiome cutané n’est pas stable : il se construit progressivement et sa maturation conditionne le développement immunitaire cutané.
– Les différences de composition selon que l’accouchement a eu lieu par voie basse ou par césarienne s’estompent au bout d’un mois,
– au cours de la première année, les staphylocoques et streptocoques sont prédominants,
– progressivement, les Actinobacteria, Proteobacteria puis Bacteroidetes s’installent,
– la biodiversité microbienne, essentielle à l’homéostasie cutanée, se consolide jusqu’à l’adolescence.
Rôles du microbiome cutané : bien plus qu’un simple locataire
Protection contre les infections
Staphylococcus epidermidis joue un rôle protecteur majeur par plusieurs mécanismes :
– compétition pour les sites d’ancrage contre les pathogènes comme Staphylococcus aureus,
– production de protéases à sérine inhibant la formation de biofilms pathogènes,
– stimulation de la synthèse kératinocytaire de peptides antimicrobiens (défensines, cathélicidines),
– production de bactériocines et d’acides gras à chaînes courtes antibactériens naturels.
Protection contre les tumeurs cutanées
S. epidermidis produirait des molécules inhibant l’activité ADN polymérase dans les cellules cutanées en cours de transformation, suggérant un effet protecteur contre les cancers cutanés UV-induits. Des recherches actives sont en cours sur ce mécanisme.
Régulation du système immunitaire cutané
Le microbiome cutané éduque et module l’immunité cutanée innée et adaptative en :
– contrôlant les pathogènes par compétition et production d’antimicrobiens,
– induisant une tolérance immunitaire envers les commensaux (évitant les réactions auto-immunes),
– modulant les réponses Th1, Th2 et Th17 selon les espèces présentes.
La réduction de la diversité microbienne cutanée est associée à de nombreuses dermatoses inflammatoires chroniques : dermatite atopique, psoriasis, rosacée, acné. Des soins d’hygiène doux, respectant le microbiome, renforcent simultanément la barrière cutanée et la barrière immunitaire.
Le microbiome intestinal : un organe à part entière
Le microbiome intestinal pèse environ 2 kilogrammes (40 % du poids fécal) et contient 50 à 60 milliards de bactéries appartenant à plus de 1 000 espèces identifiées, dont environ 160 espèces par individu.
Sa composition est unique : 1/3 des espèces est commun à tous les humains, 2/3 sont propres à chaque individu. C’est notre « code-barres bactérien », globalement stable une fois installé.
Composition par phyla dominants :
– Firmicutes : Lactobacillus, Streptococcus, Clostridium, Faecalibacterium prausnitzii — 125 espèces,
– Bacteroidetes : Bacteroides, Prevotella — 20 espèces,
– Actinobactéries : Bifidobacterium — 30 espèces.
La dysbiose intestinale (déséquilibre ou réduction de la diversité bactérienne) est associée aux maladies inflammatoires chroniques de l’intestin (MICI), aux allergies, à l’obésité, au diabète de type 2, aux maladies cardiovasculaires et aux pathologies cutanées inflammatoires.
Les trois fonctions fondamentales du microbiome intestinal
Fonction défensive
Les bactéries commensales occupent les sites d’ancrage de la muqueuse intestinale, empêchant la colonisation par les pathogènes. Elles induisent la sécrétion d’IgA sécrétoires et de peptides antimicrobiens (défensines, cathélicidines intestinales) et créent un état de tolérance anti-inflammatoire. Le GALT (Gut-Associated Lymphoid Tissue) concentre 70 % des cellules immunitaires de l’organisme le long de l’intestin.
Fonction métabolique
Le microbiome intestinal produit :
– 10 % de nos besoins énergétiques quotidiens,
– les vitamines B1, B2, B6, B9, B12 et K,
– les acides gras à chaînes courtes (AGCC) : acétate, propionate et n-butyrate par fermentation des fibres alimentaires. Le butyrate est le carburant principal des colonocytes, renforce la barrière intestinale et exerce des effets anti-inflammatoires et anticancéreux.
Il transforme également les sels biliaires, dégrade les glucides complexes des parois végétales et produit du triméthylamine (TMA) converti en TMAO hépatique — marqueur d’athérosclérose et facteur de risque cardiovasculaire.
Fonction structurale
Le microbiome maintient l’intégrité de la barrière intestinale via :
– les jonctions serrées entre entérocytes (occludine, claudine, ZO-1, ZO-2) : empêchent le passage de macromolécules, antigènes et toxines,
– le mucus intestinal (double couche dans le côlon) : support d’ancrage des bactéries bénéfiques,
– la production de zonuline régulant l’ouverture des jonctions serrées. Une hyperproduction de zonuline entraîne une hyperperméabilité intestinale (leaky gut).
L’axe intestin-peau : comment l’intestin influence la peau
L’intestin et la peau partagent de remarquables similitudes biologiques : tous deux sont des interfaces entre l’organisme et le milieu extérieur, dotés d’un réseau vasculaire dense, d’une innervation riche et de jonctions serrées analogues (jonctions des entérocytes ≃ jonctions des kératinocytes).
En cas de dermatose, on observe souvent simultanément :
– une « leaky skin » (peau perméable) : barrière cutanée altérée,
– un « leaky gut » (intestin perméable) : barrière intestinale fragilisée.
Ces deux barrières devenues poreuses favorisent le passage d’allergènes, de pathogènes et de LPS (lipopolysaccharides bactériens), entretenant une inflammation chronique systémique de bas grade.
Modes de communication de l’intestin vers la peau :
– AGCC circulants : le butyrate, l’acétate et le propionate produits par les bactéries intestinales atteignent la peau par voie sanguine et modulent directement le microbiome cutané et l’inflammation locale. Les patients acnéiques ont des taux d’AGCC significativement plus bas que les sujets sains,
– LPS bactériens : les lipopolysaccharides des bactéries Gram– franchissent la barrière intestinale perméable, activent le TLR4 (Toll-Like Receptor 4) cutané et entretiennent une inflammation systémique de bas grade impliquée dans l’acné inflammatoire, le psoriasis et la rosacée,
– Axe hormonal : les protéines laitières stimulent la sécrétion d’insuline et d’IGF-1, activant les glandes sébacées et aggravant l’acné. Les glucides raffinés à index glycémique élevé amplifient ce mécanisme via la même voie IGF-1,
– Axe immunitaire : le microbiome intestinal éduque les cellules T régulatrices, déterminant l’orientation des réponses inflammatoires cutanées (Th1, Th2, Th17),
– Axe neuroendocrinien : le microbiome intestinal interagit avec le système nerveux entérique et le cerveau (axe microbiote-intestin-cerveau), modulant indirectement la réponse au stress qui aggrave plusieurs dermatoses inflammatoires.
Microbiome et dermatoses : les associations documentées
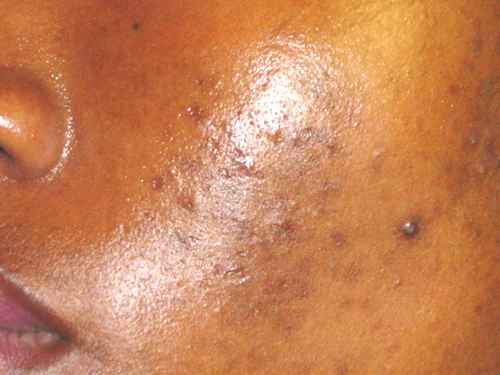
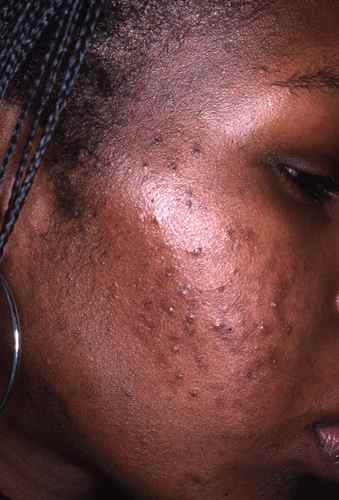
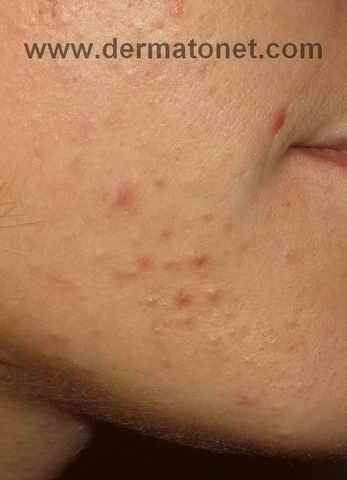
Acné et dysbiose
L’acné est la première dermatose pour laquelle une dysbiose cutanée caractérisée a été documentée : prédominance de souches virulentes de Cutibacterium acnes (phylotypes IA1 et IB) et augmentation de Staphylococcus epidermidis.
Au niveau intestinal, les patients acnéiques présentent :
– une diversité microbienne réduite avec augmentation des Firmicutes et diminution des Bacteroidetes,
– une hypochlorhydrie gastrique fréquente entraînant une mauvaise digestion des protéines et une flore de putréfaction,
– un risque accru de SIBO (Small Intestinal Bacterial Overgrowth : pullulation bactérienne de l’intestin grêle).
La Western diet (produits laitiers, sucres à IG élevé, acides gras saturés, déficit en oméga-3) est désormais reconnue comme facteur causal de l’acné via l’activation des voies IGF-1, mTORC1 et SREBP-1 stimulant l’hyperséborrhée et la prolifération de Cutibacterium acnes.
La supplémentation en Lactobacillus rhamnosus SP1 améliore l’expression des gènes cutanés impliqués dans la voie de l’insuline et réduit les lésions acnéiques.
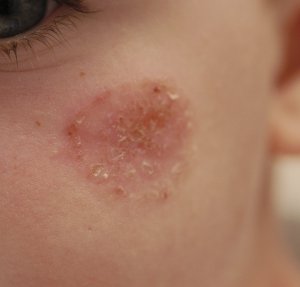
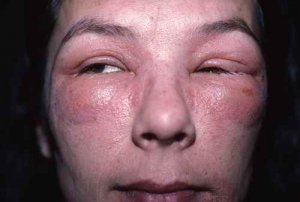
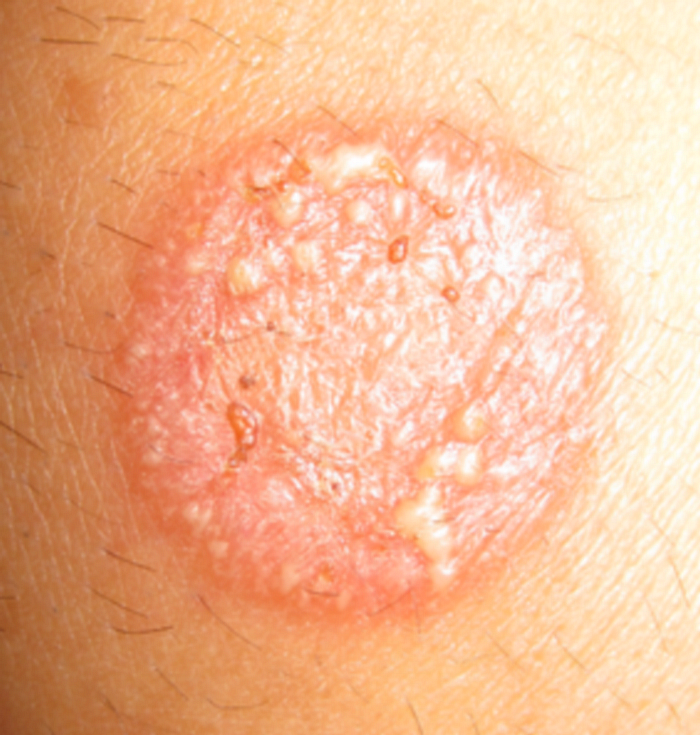
Dermatite atopique et dysbiose
Dans la dermatite atopique, le microbiome cutané est profondément perturbé avec une colonisation massive par Staphylococcus aureus, absente ou minimale sur la peau saine. S. aureus :
– dégrade les céramides et les protéines de jonction cutanée via ses protéases et céramidases,
– stimule les voies Th2 pro-atopiques,
– réduit l’activité des cellules T régulatrices.
Par ailleurs, 30 % des Caucasiens portent une mutation du gène de la filaggrine, protéine essentielle de la différenciation épidermique, aggravant la sécheresse et la perméabilité cutanée.
Au niveau intestinal, une prévalence accrue de Clostridia et une diminution de Faecalibacterium prausnitzii précèdent l’apparition de la dermatite atopique, suggérant un rôle causal. La supplémentation en probiotiques (lactobacilles et bifidobactéries) au 3e trimestre de grossesse a démontré une efficacité préventive sur la survenue de la dermatite atopique.
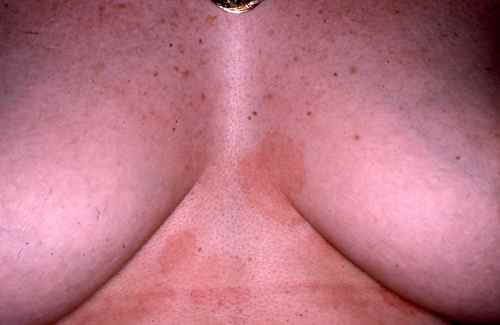
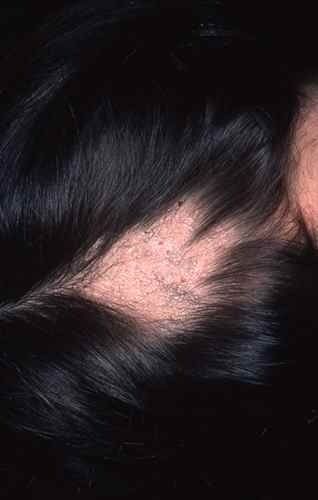
Psoriasis et dysbiose
Le psoriasis est fréquemment associé aux maladies inflammatoires intestinales (MICI). La dysbiose intestinale observée se caractérise par :
– diminution d’Akkermansia muciniphila (comme dans l’obésité et le diabète),
– diminution de Faecalibacterium prausnitzii, bactérie produisant du butyrate qui inhibe la voie inflammatoire NF-κB,
– augmentation des Firmicutes et Actinobacteria.
Les LPS bactériens issus de la dysbiose favorisent la translocation bactérienne dans le sang, entretenant l’inflammation systémique de bas grade qui alimente les poussées de psoriasis.
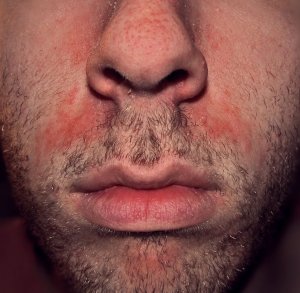
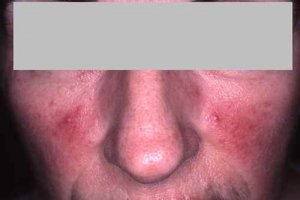
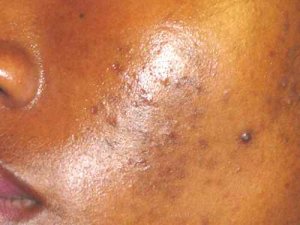
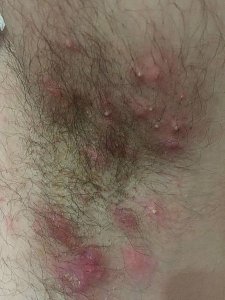
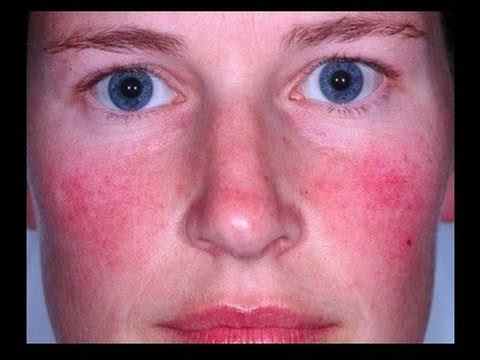
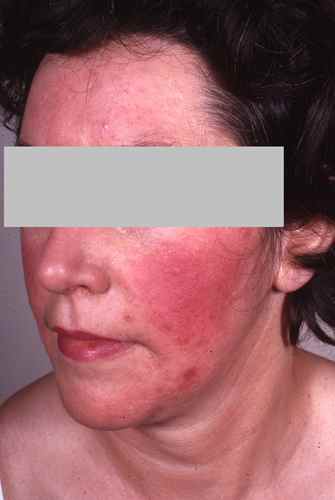
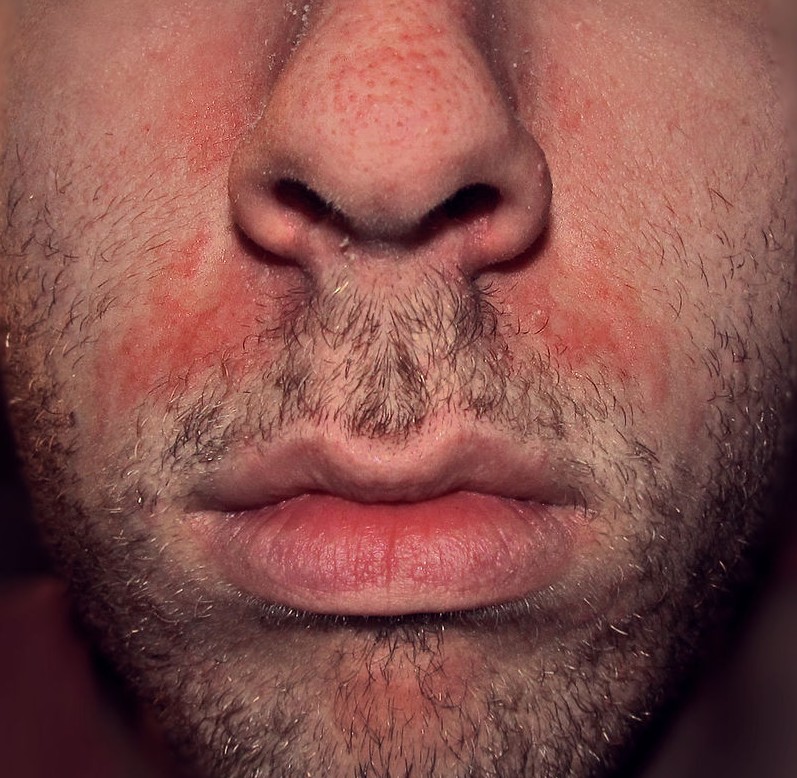
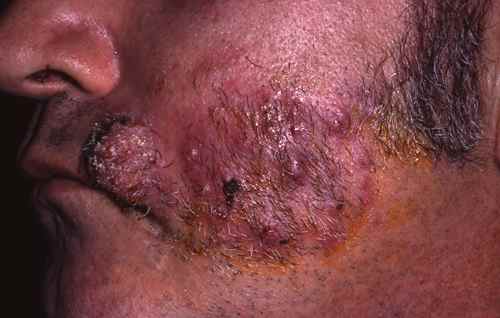
Rosacée et dysbiose
Le lien entre déséquilibre du microbiome intestinal et rosacée est établi de longue date : les signes digestifs (ballonnements, douleurs abdominales) sont fréquemment associés à la rosacée.
– La prévalence de l’infection à Helicobacter pylori est augmentée dans la rosacée,
– le SIBO (Small Intestinal Bacterial Overgrowth) est plus fréquent chez les patients atteints de rosacée,
– le traitement du SIBO par rifaximine s’est accompagné d’une réduction significative des lésions cutanées de rosacée pendant 9 mois.
Demodex folliculorum, l’acarien commensal du follicule pileux dont la densité est augmentée dans la rosacée, interagit également avec le microbiome cutané local.
Comment explorer son microbiome intestinal ?
Métagénomique (séquençage ARN 16S bactérien) :
Le séquençage à haut débit permet d’identifier 85 % des souches bactériennes anaérobies, contre seulement 25 % par la culture classique (coproculture). C’est l’examen de référence pour analyser la composition du microbiome intestinal.
Métabolome :
Quantifie les acides gras à chaînes courtes (AGCC) et évalue l’activité fonctionnelle du microbiome. Le n-butyrate est le marqueur clé de la santé de la muqueuse colique.
Métabolites organiques urinaires (MOUs) :
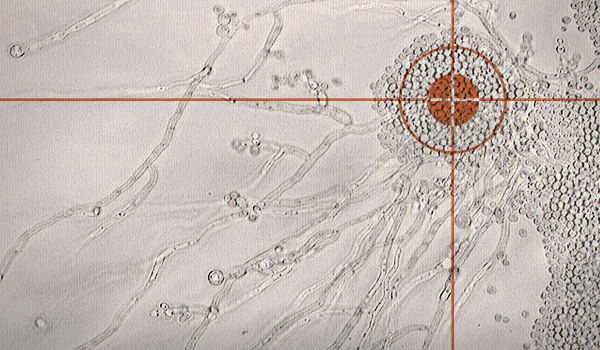
Mettent en évidence de façon spécifique et quantitative l’activité métabolique des bactéries pathogènes et des levures (Candida albicans). Trois profils sont identifiables :
– flore fongique : candidose digestive,
– flore de fermentation : mauvaise digestion des sucres → régime sans FODMAPs recommandé,
– flore de putréfaction : mauvaise digestion des protéines (Clostridium difficile possible).
Zonuline sérique :
Marqueur de la perméabilité intestinale. Son élévation signe un leaky gut et une activation de l’inflammation systémique.
Prendre soin de son microbiome pour prendre soin de sa peau
Alimentation et microbiome intestinal
– Diète méditerranéenne : légumes, fruits, légumineuses, poissons gras, huile d’olive — modèle alimentaire le mieux documenté pour la diversité microbienne intestinale,
– Prébiotiques (fibres fermentescibles) : nourrissent les bactéries bénéfiques intestinales. Sources : poireau, asperge, salsifis, oignon, ail, artichaut, chicorée, banane, avoine, riz,
– Probiotiques alimentaires : augmentent les bifidobactéries bénéfiques. Sources : yaourt nature, kéfir, choucroute, kimchi, miso, cornichons fermentés naturels,
– Réduire la Western diet : limiter les sucres à IG élevé, les produits laitiers en excès et les graisses saturées pour améliorer l’acné et les dermatoses inflammatoires,
– Oméga-3 (poissons gras, noix, graines de lin) : anti-inflammatoires, réduisent les LPS circulants.
Soins cutanés respectueux du microbiome
– Préférer les nettoyants syndets surgras (sans savon) au pH proche du pH cutané (4,5-5,5) pour ne pas perturber le microbiome résident,
– éviter les antiseptiques systématiques sur peau saine (chlorhexidine, alcool) qui éliminent indistinctement commensaux protecteurs et pathogènes,
– utiliser des émollients non comédogènes régulièrement pour renforcer la barrière cutanée et maintenir l’environnement favorable aux commensaux,
– les cosmétiques probiotiques (contenant des lysats bactériens ou des bactéries vivantes) améliorent la barrière cutanée et augmentent les peptides antimicrobiens. Des formulations à base de Lactobacillus et de Vitreoscilla filiformis montrent des résultats prometteurs dans la dermatite atopique,
– éviter les antibiotiques topiques en automédication prolongée : risque de sélection de résistances et de perturbation du microbiome résident.
Probiotiques oraux et dermatoses
– Dermatite atopique : Lactobacillus rhamnosus GG, Bifidobacterium lactis en prévention prénatale et chez le nourrisson,
– Acné : Lactobacillus rhamnosus SP1, Lactobacillus acidophilus,
– Rosacée : réduction du SIBO par rifaximine, Lactobacillus acidophilus + Bifidobacterium longum.
Questions fréquentes sur le microbiome et la peau
Peut-on analyser son microbiome cutané ?
Des tests de microbiome cutané sont proposés par certains laboratoires spécialisés (prélèvement par écouvillonnage ou bandelette cutanée avec séquençage métagénomique). Bien que scientifiquement fondés, leur utilité clinique en pratique courante reste à préciser. En dermatologie, le diagnostic repose encore principalement sur la clinique et les examens biologiques conventionnels.
Les antibiotiques abîment-ils le microbiome cutané ?
Oui, de façon transitoire pour les antibiotiques topiques et plus durable pour les antibiotiques systémiques. Une antibiothérapie systémique modifie significativement le microbiome cutané pendant plusieurs semaines à mois après l’arrêt, favorisant la colonisation par des espèces résistantes ou opportunistes. La supplémentation en probiotiques pendant et après une antibiothérapie peut atténuer ces effets.
Le stress influence-t-il le microbiome cutané ?
Oui. Le stress active l’axe hypothalamo-hypophyso-surrénalien (HHS), augmentant la production de cortisol et de neuropeptides (substance P, NGF) qui modifient directement la composition du microbiome cutané et intestinal. Le stress aggrave cliniquement l’acné, le psoriasis, la dermatite atopique et la rosacée — en partie via cet effet sur les microbiomes.
Les produits ménagers et les désinfectants abîment-ils le microbiome cutané ?
L’exposition répétée aux biocides ménagers (désinfectants, antibactériens de surface) perturbe le microbiome cutané des mains et du corps. Des études montrent une association entre usage intensif de produits antibactériens et augmentation du risque d’allergies et de dermatoses, en accord avec l’hypothèse hygiéniste : un microbiome moins diversifié, moins exposé aux micro-organismes environnementaux, entraîne une immunité moins bien régulée.
Besoin de l’avis d’un spécialiste ? Délais de rendez-vous trop longs ? Vous pouvez effectuer une téléconsultation avec le dermatologue.
En savoir plus sur la dermatite atopique,
le psoriasis,
l’acné et son lien avec l’alimentation,
la rosacée,
l’hydratation cutanée et les émollients
et la structure et le fonctionnement de la peau.









.jpg)
.jpg)